Startpagina mlochemie
Atomen kunnen bij temperatuurverhoging energie opnemen. Hierbij gaat een elektron naar een hogere schil. Het atoom is dan in "aangeslagen toestand".
{module animconcverstuiver}
Het atoom kan de energie weer afstaan door elektromagnetische straling uit te zenden. Het elektron valt daarbij terug naar zijn oorspronkelijke schil. De energie komt weer vrij maar nu dus als elektromagnetische straling. Het atoom emitteert een foton. Om atomen in aangeslagen toestand te brengen moet de temperatuur omhoog.
In een gewone vlam komen er maar weinig atomen in aangeslagen toestand. In een acetyleen-lucht-vlam van circa 2000 K zijn er maar ongeveer 20 atomen aangeslagen op elke miljard atomen. Dus 20 op 1 000 000 000.
Deze 20 zorgen voor de emissie. Maar al die niet aangeslagen atomen (1 000 000 000), die kunnen straling absorberen. Geen wonder dat AAS gevoeliger is dan vlam-AES. Geen wonder ook dat vlam-AES erg afhankelijk is van de temperauur van de vlam. Gaan we met de temperatuur 100 K omhoog dan verdubbelt de emissie!
Belangrijk is daarbij de verstuiving van het monster. Monsterduppeltjes kunnen gemaakt worden met een veel gebruikte concentrische verstuiver.
Proefondervindelijk wordt bepaald of een andere verstuiver, bijvoorbeeld de cross flow verstuiver betere resultaten geeft. Voor heel schone monsters met lage concentraties zoals in drinkwater, gebruiken we een geforceerde vernevelaar: een ultra soon verstuiver.
Emissie wordt interessant als we de temperatuur flink verhogen. In een plasma van 6000 K zijn er op elke 100 atomen 2 á 3 in aangeslagen toestand. Dan maken we gebruik van een plasma. Een ICP-spectrometer. Hier een afbeelding van een tafelmodel van Perkin Elmer.

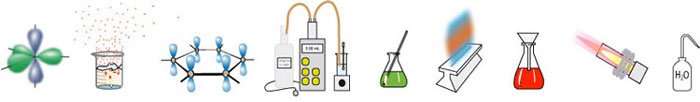
Hieronder de stralengang van dit instrument.
Wat valt op?
De emissie van de ICP-toorts wordt zowel rechtuit als zijwaarts opgevangen. De zijwaartse straling wordt gebruikt om de stand van de toorts te optimaliseren.
Via een Echelle polychromator gaat de straling naar een dispergerende spiegel die ook een deel door laat. Zichtbaar licht gaat door de "Schmidt Cross Disperser" heen. UV wordt teruggekaatst. Er is dus een CCD detector voor uv en een voor zichtbaar licht.
kruiswoord h10
{module animatoomabsorptie}
Atomen kunnen straling absorberen. Het atoom neemt een foton op. Een elektron beweegt dan naar een hoger gelegen schil. En dus naar een hoger energieniveau. Het atoom komt dan in "aangeslagen toestand". Het is wel nodig om te zorgen voor losse atomen. Dus atomen in de gasfase. Dat lukt alleen bij hoge temperatuur. De te meten stoffen moeten worden "geatomiseerd". Bij AAS gebeurt dat in een vlam of in een "oven".
Een dergelijke "grafiet oven" is maar een klein koolstof buisje. Twee van zulke buisjes staan hieronder:

De meting bij AAS gebeurt door de te meten component opgelost in een vlam te brengen of in een koolstofoventje. Door verhitting verdamt de vloeistof en komen er vrije atomen in de vlam of de oven.
Het gaat over absorptie van licht. Hierbij geldt de wet van Lambert-Beer: De extinctie is evenredig met de concentratie en de weglengte:

Hieronder een sterk vereenvoudigd schema van een AAS-spectrometer. In dit geval van Perkin Elmer.
Wat valt op?
* de monochromator komt ná de vlam (of oven)
* er zijn 8 lampen beschikbaar
* de lichtbundel loopt niet rechtlijnig via spiegels maar gaat door glasvezelkabel!

Aan video's is er veel te vinden, maar: veel van slechte kwaliteit, chaotisch, langdradig of commercieel. Een van de beste uitlegjes is nog van Katherine die je in vlot maar soms onverstaanbaar Engels uitlegt hoe het AAS apparaat er uit ziet. Toch redelijk duidelijk.
En een heel simpele demo van hoe je een monster toevoert bij vlam-AAS.
Als je het in plaatjes nog eens langs wil lopen bekijk dan deze pdf.
En verder....
Is er natuurlijk de test hoofdstuk 9 en het kruiswoord h 9.

Bij zichtbaar licht spectrometrie meet je met de lichtkleur die de stof het meest absorbeert. Dat is de complementaire kleur in de kleurencirkel.
UV-licht kun je niet zien maar je kunt er wel mee meten. Je gebruikt dan een kwarts cuvet, deze laat uv-licht doortot circa 200 nm.
Je past bij de meting de wet van Lambert-Beer toe. Deze zegt dat... de gemeten extinctie afhangt van stof-concentratie, weglengte en soort stof:
E = ε × c × l
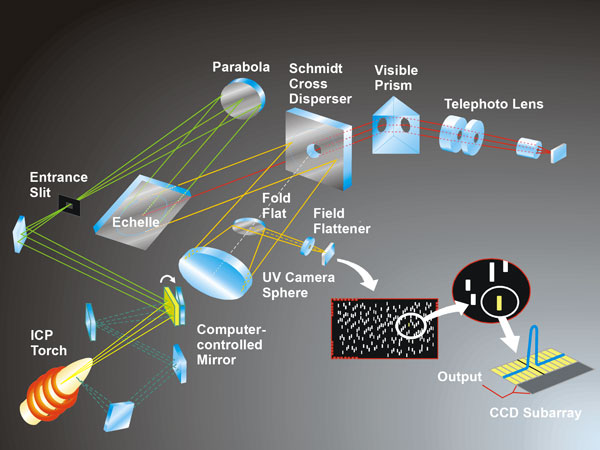
Bij een spectrometrische bepaling stel je altijd ten minste E = 0,000 in met de blanco in de lichtweg.
De fotometer zelf stelt nog T = 0,00 in bij geblokkeerde lichtweg. Bij sommige apparaten of als extra controle doe je dat zelf.
Voor de duidelijkheid :
* Onderbroken lichtweg
- er valt geen licht op de detector
- Je stelt in: T = 0,0% (Maak niet de fout hier E = 0,000 in te stellen!!!)
Deze instelling hoef je meestal niet zelf te doen. Een moderne fotometer doet dit zelf bij de opstartprocedure. Maar... het kan voorkomen dat je het toch wilt controleren. Je moet dan de lichtweg echt blokkeren met een schuifje van de fotometer of door voorwerp in de cuvethouder te plaatsen.
* Blanco in de lichtweg
- de blanco zit in de cuvet
- Iblanco is iets kleiner dan I0 maar je hoeft hier verder geen rekening mee te houden, omdat de fotometer toch rekent met Ib in plaats van de "echte" I0.
- Je stelt in: T = 100,0% of E = 0,000.
* Lichtweg met het monster in de cuvet
- monster in de cuvet
- Imonster is (veel) kleiner dan I0 of Iblanco
- T ligt tussen 0% en 100%
- je leest meestal af: Extinctie (Absorbance)
Met een animatie van de Wet van Lambert-Beer kun je hier oefenen.
Merk op dat het Engelse Absorbance in de animatie is vertaald als 'absorptie'. Dat moet natuurlijk zijn: Extinctie.
en verder...
Even nog op een rijtje de eigenschappen van de elektromagnetische golf:
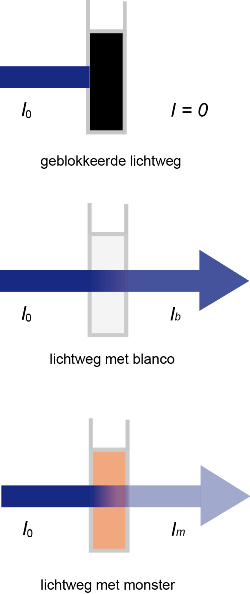
Golflengte (λ)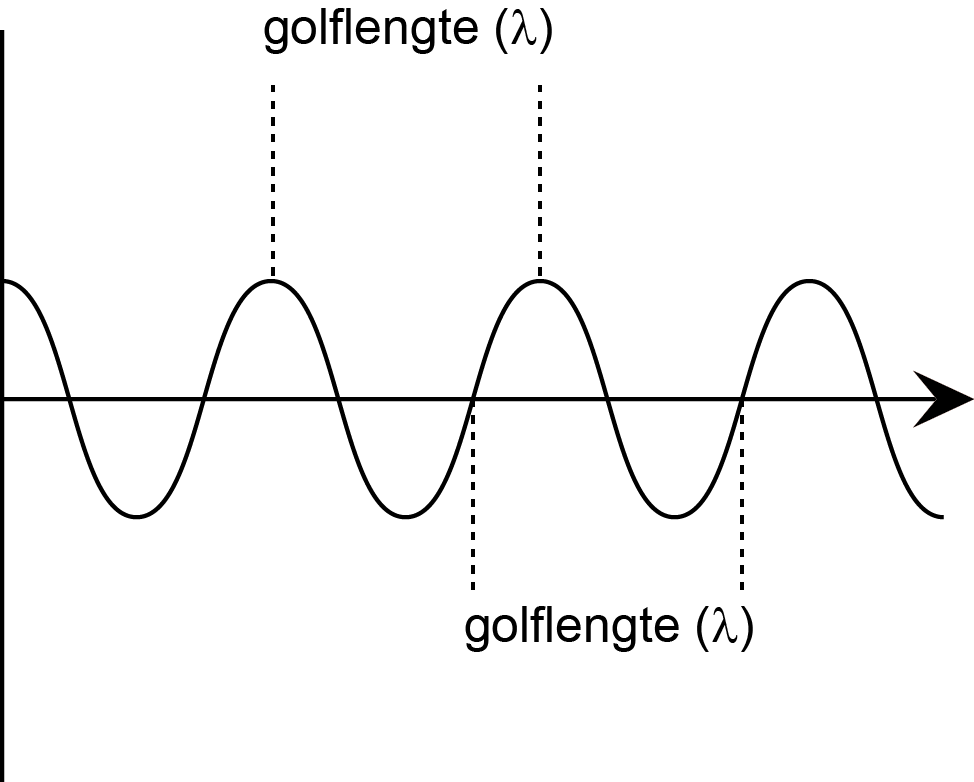
De golflengte van een golf, dus ook van een elektromagnetische, is de afstand tussen twee punten met dezelfde bewegingsfase. Bijvoorbeeld de afstand tussen 2 pieken. Of 2 dalen. Of 2 opeenvolgende punten waar de golf net omhoog gaat vanaf het midden. Het is steeds een klein stukje maar wel zo dat de hele golf er uit kan worden opgebouwd door het stukje te vermenigvuldigen. Kijk naar de afbeelding.
De golflengte is een afstand. In meter of ... mm, μm, nm ...
Golfgetal (σ)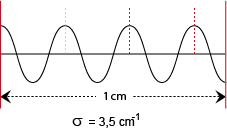
Het golfgetal is het omgekeerde van de golflengte. Je krijgt dan het aantal golven op 1 lengte-eenheid. In de spectrometire wordt dan vaak 1 cm gebruikt. Dus het golfgetal is dan het aantal golven op 1 cm. In de afbeelding is dat 3,5 golf. Dus 3,5 per cm.
Frequentie (f)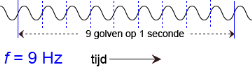
De frequentie geeft het aantal golven per tijdseenheid. We gebruiken dan eigenlijk altijd de seconde. Dus: het aantal golven per seconde. Met als eigen eenheid: Hz. Hiernaast: 9 golven per seconde is dan 9 Hz.
Foton-energie (E)
Elektromagnetische straling is "gekwantiseerd". Dat wil zeggen: de straling ontstaat uit energie-overgangen van elektronen, trillingen van moleculen enzovoorts. Maar steeds in stappen. Je zou kunnen zeggen: digitaal en niet analoog. Elke overgang heeft een energie-pakketje dat wordt opgenomen of afgestaan. Dit noemen we een foton. Een foton is dus een kleinst mogelijk stukje golf dat bij een overgang hoort. Voor veel straling zijn dan heel erg veel fotonen nodig.
Breking
Elektromagnetische straling kan breking vertonen. Als de straling schuin invalt op een andere stof waarin de straling langzamer of juist sneller beweegt dan verandert de straling van richting. Dit kennen wij vooral van zichtbaar licht dat vanuit de lucht op een transparante stof valt. Glas, water ed.
Polarisatie
Elektromagenetisch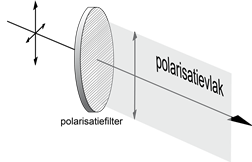 e straling is een golf. De amplitude, de golftop zeg maar, die kan elke richting hebben. Maar de straling kan ook "gepolariseerd" zijn. Gepolariseerde straling heeft maar één trilrichting.
e straling is een golf. De amplitude, de golftop zeg maar, die kan elke richting hebben. Maar de straling kan ook "gepolariseerd" zijn. Gepolariseerde straling heeft maar één trilrichting.
Buiging en interferentie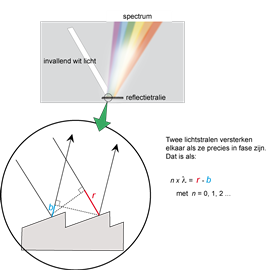
Als golven door een smalle opening gaan dan gaan ze na de opening in alle richtingen verder. Elke opening lijkt te werken als een aparte lichtbron. Dat zie je ook als je golven laat terugkaatsen op een oppervlak met fijne ribbels of groeven. Elke groef lijkt dan te werken als een apart lichtbronnetje. Na de terugkaatsing ontstaat dan interferentie. Golven die juist in fase zijn versterken elkaar. Golven die juist in tegenfase zijn doven elkaar uit. Dit proces verloopt voor iedere golflengte apart en onder een steeds iets andere terugkaatstingshoek. Zo kun je uit wit licht een regenboog maken. Hiervan wordt gebruik gemaakt in een monochromator.
Monochromator
{module animmonochromator}
Buiging en interferentie met een reflectie rooster wordt toegepast in een monochromator. Deze maakt van wit licht een spectrum. Je kunt door het rooster (of een spiegel) te draaien de kleur van het licht dat je gebruikt, regelen.
Straling en moleculen
Laat je em-straling op moleculen vallen dan kan de straling geabsorbeerd worden. Afhankelijk van de frequentie van de straling neemt het molecuul energie op. Deze energie-opname kan op drie manieren:
door de elektronen, door vibratie of rotatie. Hieronder staat een animatie waarin dat wordt zichtbaar gemaakt. Je kunt de soort straling kiezen, het molecuul kiezen en de lamp-energie regelen.
Wat doet......
a een microgolf met ozon, en water?
b infrarood met koolstofdioxide, met ozon, met water?
c UV met stikstofdioxide, met zuurstof?
En verder.....