Startpagina mlochemie
Systematische Naamgeving
Voor dezelfde stof bestaan verschillende namen. Voor ethanol kennen we bijvoorbeeld de oude naam ‘wijngeest’. En de alledaagse: ‘alcohol’ of ‘ethylalcohol’. Een naam kan traditioneel zijn of verbonden aan een beroepsgroep. Zo spreken biochemici over ‘lactaat’ als zij ‘melkzuur’ bedoelen (of eigenlijk: ‘2-hydroxypropaanzuur’).
De ‘International Union of Pure and Applied Chemistry’ (IUPAC) probeert hierin orde te scheppen. De IUPAC maakt onderscheid tussen:
-triviale naam, veel gebruikte vaak traditionele naam,
-semi-systematische naam, dan zit er enige logica in de naam, bijvoorbeeld: ethylalcohol,
-systematische naam, deze is afgeleid van de structuurformule.
De systematische naam beschrijft de molecuulstructuur.
In het boek Organische chemie voor het beroepsonderwijs bespreken we bij iedere homologe reeks de gangbare triviale namen. Bovendien de de belangrijkste richtlijnenen voor de systematische naam. Een heel algemene richtlijn volgt hieronder.
Globale regels voor de systematische naam.
De hoofdnaam wordt bepaald door de langste niet-vertakte keten waarin de functionele groep zit. Is er geen functionele groep dan wordt de naam van de langste keten de alkaannaam. Het eerste deel (blauw) is de ‘stam’:
CH4 methaan
C2H6 ethaan
C3H8 propaan
C4H10 butaan
C5H12 pentaan
C6H14 hexaan
C7H16 heptaan
C8H18 octaan
C9H20 nonaan
C10H22 decaan
- Met 1 dubbele binding wordt de naam: stam+een, dus etheen, propeen enz.
- Met 2 dubbele bindingen: stam+adieen, dus butadieen, pentadieen enz.
- Met 1 drievoudige binding wordt de naam: stam+yn, dus ethyn, propyn enz.
- Met 2 drievoudige bindingen: stam+adiyn, dus butadiyn, pentadiyn enz.
- Komen drievoudige en dubbele binding samen voor dan is de nummering zo laag mogelijk, met voorkeur voor het laagste nummer voor –een.voorbeeld:
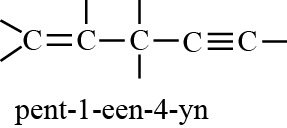
- Een cyclische verbinding krijgt ‘cyclo-‘ als voorvoegsel: cyclo-hexaan, cyclo-hexeen enz.
- De stamnaam bij aromaten en polycyclische verbindingen is afgeleid van de ringstructuur. Deze heeft dan een eigen stamnaam. Bijvoorbeeld: benzeen, naftaleen, anthraceen, enz. Vertakkingen van de koolstofketen worden als substituent voor de hoofdnaam vermeld met de uitgang -yl:
CH4 methaan -CH3 methyl
C2H6 ethaan -C2H5 ethyl
C3H8 propaan -C3H7 propyl
C2H4 etheen -C2H3 ethenyl
C3H6 propeen -C3H5 propenyl
- Zit er een functionele groep in de keten dan krijgt de langste keten met functionele groep een afgeleide naam. De functionele groep die aan het eind van de hoofdnaam wordt geplaatst is de hoofdgroep.
- De plaats van een functionele groep wordt met een nummer aangegeven. Dit plaats-nummer wordt vlak voor de uitgang gezet:

- Zijn er meer functionele groepen dan krijgen deze ook plaats-nummers. Dan worden nummer en naam vóór de hoofdnaam geplaatst.
Voorbeeld:

- In onderstaande tabel staat een aantal veel voorkomende groepen van boven naar beneden gerangschikt naar hoofdgroep-voorkeur.
- Dus bijvoorbeeld: de uitgang –zuur heeft voorrang boven de uitgang –al voor de hoofdnaam (als gekozen moet worden).
- Als het plaatsnummer overbodig is dan laten we het weg:niet: 4-broom-2-oxo-pentaan-1-zuur maar: 4-broom-2-oxo-pentaanzuur
niet: propaan-2-on maar: propanon
niet: hexaan-1-al maar: hexanal
Voorkeur van boven naar beneden voor de bepaling van de hoofdnaam-uitgang.
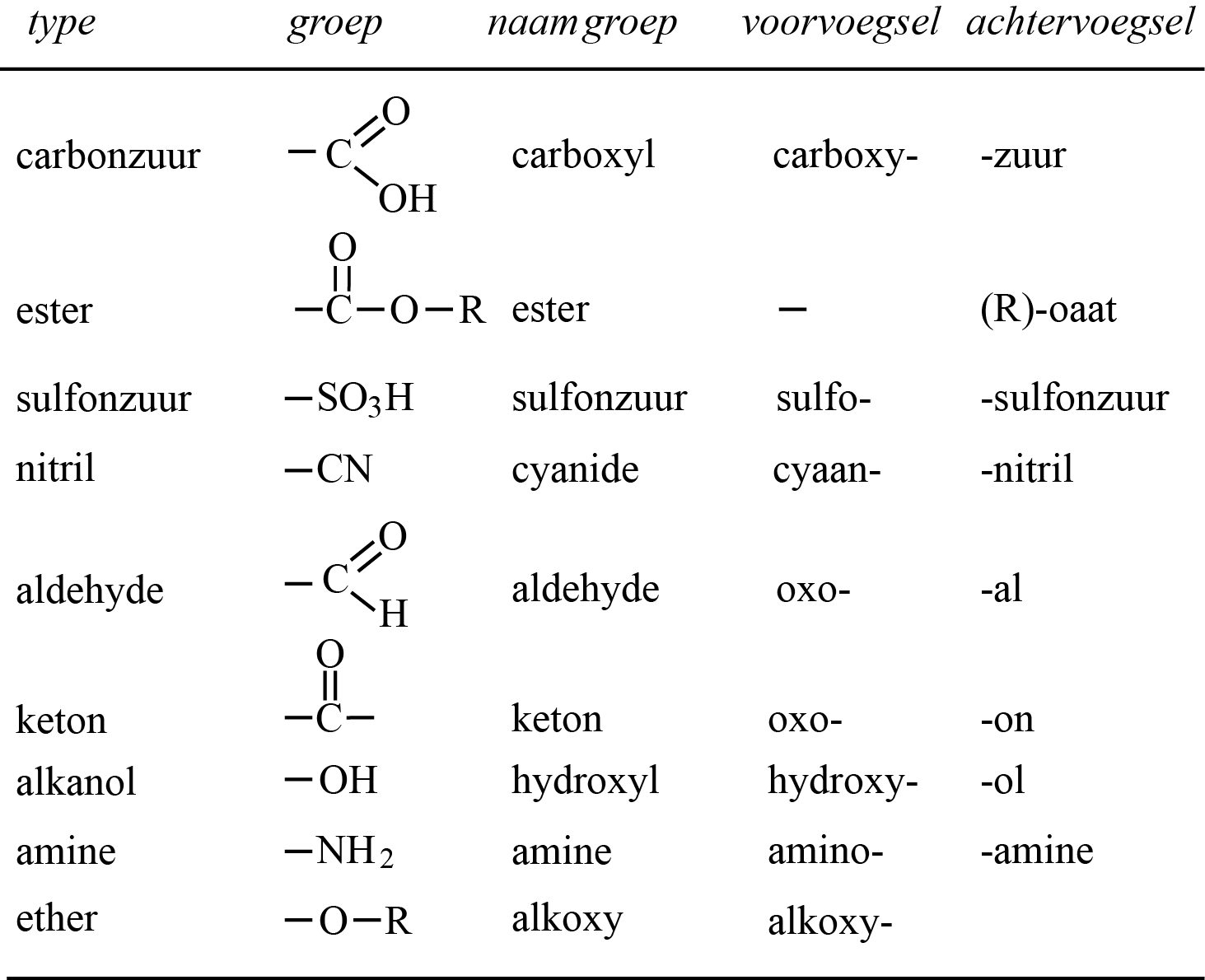
- Sommige groepen worden alleen als voorvoegsel genoemd, bijvoorbeeld de nitro-groep en de halogenen.
- Het aantal van dezelfde groep geven we aan met voorvoegsels: mono, di, tri, tetra enz.
- Bij meer dan één functionele groep wordt de nummering zó gekozen dat de nummers zo laag mogelijk zijn. Bij vergelijking van twee mogelijkheden van nummering worden de plaatsnummers van beide nummeringen oplopend op een rij gezet. Vervolgens is die nummering het laagst, waarbij bij het eerst optredende verschil, het kleinste getal staat.
Vergelijk A 2,3,6,7 met B 3,4,6,7
A is het laagst want bij het eerste verschil is 2 het kleinst.
Vergelijk C 2,3,6,8 met D 2,4,5,7
C het laagst want bij het eerste verschil is 3 het kleinst.
Je krijgt de volledige naam als je alle functionele groepen en hun plaatsnummers in volgorde zet:
zijketens, functionele groepen -- stamnaam -- dubbele, driev. binding -- uitgang hoofdgroep
Hierbij:
- nummers scheiden met komma’s: 2,3,4-
- voorvoegsels als: cyclo, di, tri, cis, trans enz scheiden met liggend streepje: tri-methylamine
- namen van groepen aan de naam schrijven: 2-methylpentaan, 2-aminobutaan-1-ol
Werkwijze bij de bepaling van een systematische naam
- Bepaal de stam, dus: langste keten met meeste functionele groepen en dubbele / drievoudige bindingen.
- Bepaal welke functionele groepen benoemd moeten worden met: tussenvoegel, voorvoegsel en of uitgang.
- Geef de functionele groepen ieder een plaatsnummer.
Voorbeeld
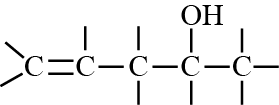
Stam: pent
Hoofdgroep: -OH uitgang: -ol plaats: 2
Subgroep: dubbele binding uitgang: -een plaats: 4
Naam: pent-4-een-2-ol
Voorbeeld

Stam: hept
Hoofdgroep: =O uitgang: -al plaats: 1
Subgroepen: -OH voorvoegsel: hydroxy plaats: 6
-C2H5 voorvoegsel: ethyl plaats: 3
-C6H11 voorvoegsel: cyclohexyl plaats: 5
dubbele binding: uitgang: -een plaats: 2
Naam: 3-ethyl-5-cyclohexyl-6-hydroxyhept-2-een-1-al
Het plaatsnummer 1 voor de uitgang -al laten we weg, want dit is overbodig:
3-ethyl-5-cyclohexyl-6-hydroxyhept-2-enal
Systematische namen zijn vaak ongemakkelijk. Niemand zegt “diwaterstofmonooxide” als hij water bedoelt. Of wat dacht je van de systematische naam van cholesterol (tabel)?
In principe is de systematische naam meteen de IUPAC voorkeursnaam: Preferred IUPAC Name. Afkorting: PIN. Maar soms is de triviale naam zo ingeburgerd dat deze de voorkeur krijgt. Zie onderstaande tabel.
Een aantal niet-systematische voorkeursnamen:
| PIN* | systematisch |
| acetyleen | ethyn |
| aniline | fenylamine |
| azijnzuur | ethaanzuur |
| benzoëzuur | benzeencarbonzuur |
| cholesterol |
10,13-dimethyl-17-(6-methylheptan-2-yl)- 2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro- 1H-cyclopentafenantren-3-ol |
| fenol | hydroxybenzeen |
| formaldehyde | methanal |
| mierenzuur | methaanzuur |
| oxaalzuur |
ethaandizuur |
| styreen | ethenylbenzeen |
| tolueen |
methylbenzeen |
| ureum | diaminomethanal |
*Voorkeursnamen ontleend aan Gids voor de IUPAC-nomenclatuur van organische verbindingen 2010 KNCV.
Structuurformules met ChemSketch
Stel je wilt een nette structuurformule voor in een Word-document of voor in een verslag of voor in een presentatie. Dan kun je die structuurformule met de hand tekenen. Als je netjes tekent is dat een prima optie. Maar veel chemici werken met computerprogramma's waarmee je vlot de moeilijkste structuren maakt. Een belangrijk voordeel is ook dat veel structuren al voor je klaar staan in het programma. Sommige van die programma's zijn ook voor scholieren en studenten beschikbaar. Gratis. Het zijn dan uitgeklede versies maar je kunt er toch veel mee.
Er zijn verschillende tekenprogramma's op het web te vinden: ChemDraw (betaald), ChemTube3D, AccelrysDraw, ChemSketch, MolView en meer. MolView is relatief eenvoudig (en dus beperkt) maar je kan er ook mee werken op telefoon of tablet.
ChemSketch is uitgebreider. Je kan er dus meer mee. Hieronder enige hulp.
- Handleiding voor de download procedure
-
Enige info over de bestandsformaten: Starten en opslaan
-
Beknopte handleiding voor het het maken van structuurformules
-
Voorbeeld voor het maken van een reactievergelijking.
-
Maken van ruimtelijke modellen.
Plastics, kunststoffen of polymeren ...
We bedoelen steeds hetzelfde: macromoleculaire stoffen die zijn gemaakt uit monomeren. Monomeren zijn kleine moleculen. Deze monomeren zijn dan moleculen die zich kunnen verenigen tot grote moleculen. Door het aaneenrijgen van monomeren ontstaat een polymeer.
Zou je in een kunststoffenlaboratorium komen te werken, dan moet je niet gek opkijken als je werkzaamheden heel anders zijn dan tijdens de opleiding. Voor de kwaliteitscontrole van kunststoffen worden vooral veel fysische eigenschappen gemeten.
Je moet dan denken aan:
- warmtegeleiding
- slagvastheid
- brandbaarheid
- scheursterkte
- treksterkte
- krasvastheid
- uv-bestendigheid
Veel (chemische polymeren) worden gemaakt door in hoofdzaak twee bereidingswijzen: radicaalpolymerisatie en condensatiepolymerisatie.
Radicaalpolymerisatie
Condensatiepolymerisatie

Duurzaamheid
Kunststoffen hebben niet zo een goede naam als het gaat om de aanwezigheid in het milieu. 
Het duurt erg lang voordat plastic is afgebroken. Hoewel: echt duurzaam zijn de meeste plastics ook niet. Zie het schakeldoosje in de afbeelding. Het is vooral de invloed van UV-straling in zonlicht die het materiaal aantast.
Maar het duurt wel erg lang voordat plastic op deze wijze is afgebroken. En ... er wordt enorm veel plastic gebruikt. De oplossing is recycling. Vooral van kunststoffen die goed gescheiden opgehaald kunnen worden. Veel PET-flessen krijgen zo een tweede of derde leven. Zie Canadees filmpje.
Een andere oplossing, die bijvoorbeeld voor weggooi-bestek wordt gebruikt, is biologisch afbreekbaar plastic. Dit wordt gemaakt uit zetmeel en is in principe een polyester van melkzuur:
|
|
|
Het weggooi-bestek bestaat uit polymelkzuur. PLA: polyacticacid. (CPLA ).
Interessant is ook de toepassing van polymelkzuur bij chirurgische operaties. Het polymelkzuur wordt langzaam door het lichaam opgenomen. Hechtdraad, maar ook pinnen en bouten hoeven niet meer door de chirurg verwijderd te worden.
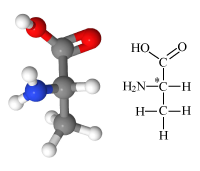 Aminozuren
Aminozuren
De verschillende zijgroepen rood: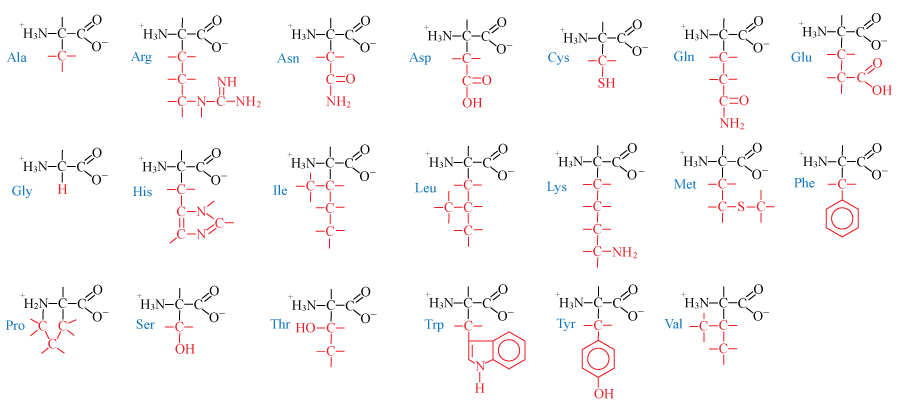
Eiwit
Een eiwit ontstaat dus door koppeling van aminozuren door middel van de amidebinding. De volgorde van de aminozuren geeft de 'primaire structuur'. Als voorbeeld, in de onderstaande afbeelding een 'heptapeptide'. 
Eiwitten rollen in schroefvorm (helix) op of liggen in laagjes op elkaar (vouwblad). Ook kunnen verschillende eiwitten in collageen-structuur rond elkaar gedraaid zijn. Spierweefsel, huid en haar. We spreken dan over de secundaire structuur.
Dat er zoveel aandacht voor het structuurniveau is komt doordat we het hier hebben over biologische moleculen. De ruimtelijke structuur is dan heel belangrijk. Een eiwit kan zijn biochemische functie alleen vervullen dankzij zijn vorm.
De structuurniveaus nog eens uitgelegd via een linkje naar Al je vragen
Als de structuur zo belangrijk is, dan zullen veranderingen in de structuur dat ook wel zijn. Een eiwit kun je "denatureren". Dit betekent: van ruimtelijke structuur doen veranderen. Hierbij verliest het eiwit zijn oorspronkelijke functie. Oplosbare eiwitten worden onoplosbaar.
Een voorbeeld van denatureren is het koken van een ei. Maar in plaats van temperatuur verhogen kun je ei-eiwit ook denatureren door toevoeging van bijvoorbeeld zuur. Dit wordt gedemonstreerd in deze video.
Bij het denatureren komen apolaire zijgroepen die naar de binnenkant van het eiwit geplaatst waren, naar buiten. Het eiwit wordt daardoor in water minder oplosbaar.
Genetische code
De aanmaak van eiwit in levende cellen gebeurt met de chemische code in DNA als recept. Het DNA bevat de basen Thymine, Adenine, Cytosine en Guanine. Drie van deze basen op een rij vormen een codon. Het codon is de codering voor een aminozuur. De basen koppelen in DNA zoals in de afbeelding:
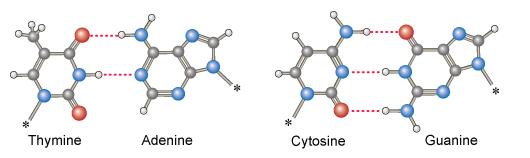
Alle eiwitten van een organisme staan geprogrammeerd in het DNA van dat organisme. Zo ook van de mens. Het DNA-profiel wordt gebruikt om verwantschap vast te stellen.